[本站讯]近日,山东大学药学院姜新义教授团队联合齐鲁医院荆卫强和李涛教授团队在Cell Stem Cell在线发表题为“In vivo CAR-Tfh Cell reprogramming restores tolerance in a mouse model of Autoimmune Hepatitis”的研究论文。本研究提出了CAR-T细胞体内编辑应用的一种新型构建方案,也为自身免疫性疾病的机制导向性干预提供了具有模块化拓展潜力的新策略。山东大学姜新义、荆卫强、李涛为共同通讯作者,药学院博士生郑作林和刘颖为共同第一作者。
自身免疫性疾病通常并非由单一免疫细胞异常所致,而是T细胞、B细胞等多种免疫成分协同失衡的结果。二型自身免疫性肝炎(AIH-II)目前主要依赖糖皮质激素及免疫抑制剂治疗,但长期应用仍面临感染风险增加、代谢不良反应及患者进展至肝移植等临床挑战。Tfh是AIH-II免疫调控网络中的关键节点,因此被认为是连接致病性免疫应答与免疫耐受重建的重要干预靶点。
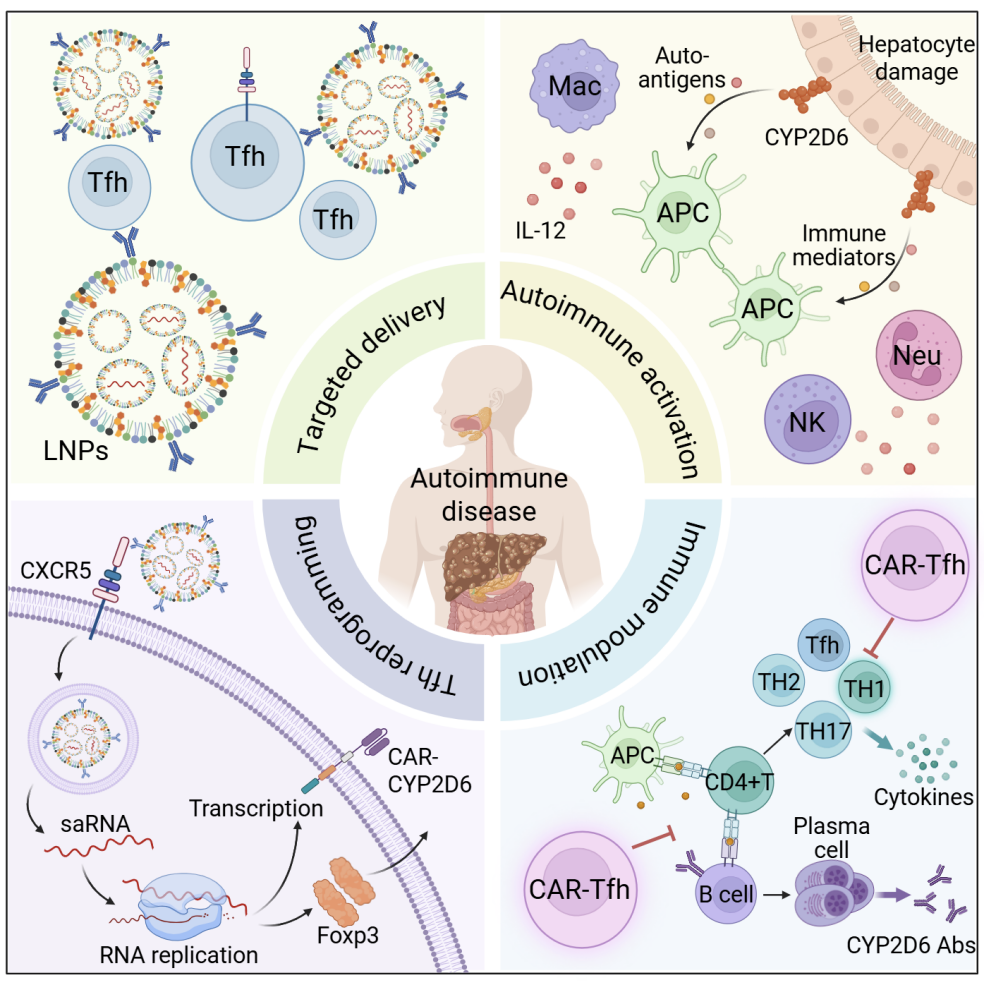
该研究建立了一种体内原位滤泡辅助T(Tfh)细胞重编程策略,可在体内原位生成兼具抗原识别与免疫调节功能的嵌合抗原受体Tfh(CAR-Tfh)细胞,并在自身免疫性肝炎模型中实现对异常免疫攻击与肝脏炎症的协同抑制。研究开发了基于色氨酸来源脂质纳米颗粒的体内递送体系,并整合自扩增RNA(saRNA)策略,提升了核酸分子体内递送效率并延长其表达持续时间。在此基础上,研究以AIH-II为疾病模型,围绕关键自身抗原CYP2D6构建抗原特异性CAR识别模块,并结合Foxp3介导的调节性程序重塑,实现了Tfh细胞向CAR-Tfh细胞的体内重编程。在AIH-II小鼠模型中,原位生成的CAR-Tfh细胞表现出抗原特异性识别能力,并对肝脏免疫微环境产生整体调控效应。研究显示,CAR-Tfh通过抑制异常活化的致病性T细胞反应,削弱B细胞活化及自身抗体相关通路,促进肝脏免疫环境向耐受状态恢复,并同步改善多项自身免疫性肝损伤指标。
该研究工作得到国家自然科学基金杰出青年基金、国家重点研发计划及山东省自然科学基金等项目资助。
